Max Planck Research Group - Magnetische Resonanz Komplexer Materialien und Katalysatoren
Prof. Dr. Thomas Wiegand - Magnetische Resonanz Komplexer Materialien und Katalysatoren
- Prof. Dr. Thomas Wiegand
- Forschungsgruppenleiter
- Magnetische Resonanz Komplexer Materialien und Katalysatoren
- +49 (0)241 80 26420
- thomas.wiegand(at)cec.mpg.de
Vita
| Diploma | Chemistry, Westfälische-Wilhelms Universität Münster, Germany (2010) |
| PhD Thesis | Prof. Hellmut Eckert, Westfälische-Wilhelms Universität Münster, Germany/ Institute of Physical Chemistry (2010-2013) |
| PostDoc | Prof. Hellmut Eckert, Westfälische-Wilhelms Universität Münster, Germany/ Institute of Physical Chemistry (2013-2014) |
| PostDoc | Prof. Beat H. Meier, ETH Zürich, Switzerland/ Laboratory of Physical Chemistry (2014-2020) |
| Habilitation | ETH Zürich, Switzerland/ Laboratory of Physical Chemistry (2019) |
| Venia Legendi | ETH Zürich, Switzerland/ Laboratory of Physical Chemistry (2020) |
| Oberassistent/Privatdozent | ETH Zürich, Switzerland/ Laboratory of Physical Chemistry (2020-2021) |
| Research Group Leader | “Magnetic resonance of complex materials and catalysts”, MPI CEC (since 2021) |
| W2-Heisenberg-Professor | “Magnetic resonance of complex materials and catalysts”, MPI CEC/RWTH Aachen (since 2021) |
Gruppenmitglieder
Publications
Full publications list | ORCID | Researcher ID / Publons
- Silva, I. d. A., Bartalucci, E., Bolm, C., Wiegand, T. (2023). Opportunities and Challenges in Applying Solid-State NMR Spectroscopy in Organic Mechanochemistry. ADVANCED MATERIALS. doi:10.1002/adma.202304092.
- Sodreau, A., Zahedi, H. G., Dervisoglu, R., Kang, L., Menten, J., Zenner, J., Terefenko, N., DeBeer, S., Wiegand, T., Bordet, A., Leitner, W. (2023). A Simple and Versatile Approach for the Low-Temperature Synthesis of Transition Metal Phosphide Nanoparticles from Metal Chloride Complexes and P(SiMe3)3. ADVANCED MATERIALS. 2306621 (1-9) doi:10.1002/adma.202306621.
- Rout, S. K., Cadalbert, R., Schröder, N., Wang, J., Zehnder, J., Gampp, O., Wiegand, T., Güntert, P., Klingler, D., Kreutz, C., Knörlein, A., Hall, J., Greenwald, J., Riek, R. (2023). An Analysis of Nucleotide-Amyloid Interactions Reveals Selective Binding to Codon-Sized RNA. Journal of the American Chemical Society, 145(40), 21915-21924. doi:10.1021/jacs.3c06287.
- Callon, M., Luder, D., Malär, A. A., Wiegand, T., Rimal, V., Lecoq, L., Böckmann, A., Samoson, A., Meier, B. H. (2023). High and fast: NMR protein-proton side-chain assignments at 160 kHz and 1.2 GHz. CHEMICAL SCIENCE, 14(39), 10824-10834. doi:10.1039/d3sc03539e.
- Zhang, Y., El Sayed, S., Kang, L., Sanger, M., Wiegand, T., Jessop, P. G., DeBeer, S., Bordet, A., Leitner, W. (2023). Adaptive Catalysts for the Selective Hydrogenation of Bicyclic Heteroaromatics using Ruthenium Nanoparticles on a CO2-Responsive Support. Angewandte Chemie, International Edition in English, (XX): e202311427, pp. x-xx. doi:10.1002/anie.202311427.
- Pfister, S., Rabl, J., Wiegand, T., Mattei, S., Malaer, A. A., Lecoq, L., Seitz, S., Bartenschlager, R., Boeckmann, A., Nassal, M., Boehringer, D., Meier, B. H. (2023). Structural conservation of HBV-like capsid proteins over hundreds of millions of years despite the shift from non-enveloped to enveloped life-style. Nature Communications, (14): 1574, pp. 1-15. doi:10.1038/s41467-023-37068-w.
- Lipinski, W. P. P., Zehnder, J., Abbas, M., Güntert, P., Spruijt, E., Wiegand, T. (2023). Fibrils Emerging from Droplets: Molecular Guiding Principles behind Phase Transitions of a Short Peptide-Based Condensate Studied by Solid-State NMR. Chemistry – A European Journal,(29) e202301159, pp. 1-11. doi:10.1002/chem.202301159.
- Bartalucci, E., Malär, A. A. A., Mehnert, A., Büning, J. B. K. B., Günzel, L., Icker, M., Börner, M., Wiebeler, C., Meier, B. H. H., Grimme, S., Kersting, B., Wiegand, T. (2023). Probing a Hydrogen-pi Interaction Involving a Trapped Water Molecule in the Solid State. Angewandte Chemie, International Edition in English, (62), 1-10,e2022177 . doi:10.1002/anie.202217725.
- Bartalucci, E., Luder, D. J., Terefenko, N., Malär, A. A., Bolm, C., Ernst, M., Wiegand, T. (2023). The effect of methyl group rotation on H-1-H-1 solid-state NMR spin-diffusion spectra. Physical Chemistry Chemical Physics, (25), 19501-19511. doi:10.1039/d3cp02323k.
- Bartalucci, E., Schumacher, C., Hendrickx, L., Puccetti, F., d'Anciaes Almeida Silva, I., Dervisoglu, R., Puttreddy, R., Bolm, C., Wiegand, T. (2023). Disentangling the Effect of Pressure and Mixing on a Mechanochemical Bromination Reaction by Solid-State NMR Spectroscopy. Chemistry – A European Journal, e202203466, pp. 1-12. doi:10.1002/chem.202203466.
- Lacabanne, D., Wiegand, T., Di Cesare, M., Orelle, C., Ernst, M., Jault, J.-M., Meier, B. H., Boeckmann, A. (2022). Solid-State NMR Reveals Asymmetric ATP Hydrolysis in the Multidrug ABC Transporter BmrA. Journal of the American Chemical Society, 144(27), 12431-12442. doi:10.1021/jacs.2c04287.
- Malär, A. A., Sun, Q., Zehnder, J., Kehr, G., Erker, G., Wiegand, T. (2022). Proton-phosphorous connectivities revealed by high-resolution proton-detected solid-state NMR. Physical Chemistry Chemical Physics, 24(13), 7768-7778. doi:10.1039/d2cp00616b.
- Zehnder, J.; Cadalbert, R.; Yulikov, M.; Künze, G.; Wiegand, T. (2021) Paramagnetic spin labeling of a bacterial DnaB helicase for solid-state NMR, J. Magn. Reson., 332, 107075, DOI:10.1016/j.jmr.2021.107075
- Malär, A.A., Wili, N., Völker, L.A., Kozlova, M.I., Cadalbert, R., Däpp, A., Weber, M. E., Zehnder, J. , Jeschke, G. , Eckert, H. , Böckmann, A. , Klose, D. , Mulkidjanian, A.Y., Meier, B.H. , Wiegand, T. (2021) Spectroscopic glimpses of the transition state of ATP hydrolysis trapped in a bacterial DnaB helicase, Nat. Commun., 12, 5293 doi.org/10.1038/s41467-021-25599-z
- Chávez, M., Wiegand, T., Malär, A. A., Meier, B. H. , Ernst, M.(2021) Residual Linewidth in Magic-Angle Spinning Proton Solid-State NMR, Magnetic Resonance, 2, 499-509. doi.org/10.5194/mr-2-499-2021
- Callon, M., Malär, A.A., Pfister, S., Rimal, V., Weber, M. E., Wiegand, T., Zehnder, J., Chavez, M., Deb, R., Däpp, A., Cadalbert, R., Fogeron, M.-L., Zyla, D., Hunkeler, A., Lecoq, L., Torosyan, A., Wang, S., Jonas, S., Glockshuber, R., Ernst, M., Böckmann, A., Meier, B.H. (2021) Biomolecular solid-state NMR spectroscopy at 1200 MHz: the gain in resolution, J. Biomol. NMR, 75, 255-272. doi.org/10.1007/s10858-021-00373-x
- Malär, A.A,, Völker, L.A.,Cadalbert, R., Ernst, M., Böckmann,A, Meier,B.H., Wiegand,T. (2021) Temperature-dependent solid-state NMR proton chemical-shift values and hydrogen bonding, J. Phys. Chem. B, 2021, 125, 6222-6230 doi/pdf/10.1021/acs.jpcb.1c04061
- Zehnder, J., Cadalbert, R., Terradot, L., Ernst, M., Böckmann, A., Güntert, P., Meier, B.H., Wiegand, T. (2021) Paramagnetic solid-state NMR to localize the metal-ion cofactor in an oligomeric DnaB helicase, Chemistry 27, 7745-7755 doi.org/10.1002/chem.202100462
- Lecoq, L., Wang, S., Dujardin, M., Zimmermann, P., Schuster, L., Fogeron, M.-L, Briday, M., Schledorn, M., Wiegand, T., Cole, A.L, Montserrat, R., Bressanelli, S., Meier, B.H., Nassal, M., Böckmann A. (2021) A pocket-factor-triggered conformational switch in the hepatitis B virus capsid, PNAS, 118, e2022464118. doi.org/10.1073/pnas.2022464118
- Kumari, P. , Gosh, D. , Vanas, A. ,. Fleischmann, Y, Wiegand, T. , Jeschke, G. , Riek, R. Eichmann, C.(2021) Structural Insights into α-Synuclein Monomer-Fibril Interactions, PNAS, 118, e2012171118. doi: 10.1073/pnas.2012171118
- Lacabanne, D.; Boudet, J.; Malär, A. A. ; Wu, P. ; Cadalbert, R. ; Salmon, L.; Allain, F. H.-T. ; Meier, B. H.; Wiegand, T. (2020) Protein side-chain-DNA contacts probed by fast magic-angle spinning NMR. J. Phys. Chem. B (124) 11089-11097 doi.org/10.1021/acs.jpcb.0c08150
- Wiegand, T.; Malär, A. A.; Cadalbert, R.; Ernst, M.; Böckmann, A.; Meier, B.H. (2020) Asparagine and glutamine side-chains and ladders in HET-s(218-289) amyloid fibrils studied by fast magic-angle spinning NMR. Frontiers Mol. Biosc.(7) 582033 doi.org/10.3389/fmolb.2020.582033
- Wiegand, T.; Lacabanne, D.; Torosyan, A.; Boudet, J.; Cadalbert, R.; Allain, F. H.-T. ; Meier, B. H.; Böckmann, A. (2020) Sedimentation yields long-term stable protein samples as shown by solid-state NMR. Frontiers Mol. Biosc. (7) 17 DOI: 10.3389/fmolb.2020.00017
- Wiegand, T.; Schledorn, M.; Malär, A. A. R. Cadalbert, R.; Däpp, A.; Terradot, L.; Meier, B. H.; Böckmann, A. (2020) Nucleotide binding modes in a motor protein revealed by 31P- and 1H-detected MAS solid-state NMR . ChemBioChem (21) 324-330 DOI: 10.1002/cbic.201900439
- Torosyan, A; , Wiegand.T ; Schledorn, M.; Klose, D.; Güntert, P.; Böckmann, A.; Meier, B. H. (2019) Including protons in solid-state NMR resonance assignment and secondary structure analysis: The example of RNA polymerase II subunits Rpo4/7. Frontiers Mol. Biosc. (6) 100. doi.org/10.3389/fmolb.2019.00100
- Malär, A. A.; Smith-Penzel, S.; Camenisch, G.-M. ; Wiegand, T.; Samoson, A.; Böckmann, A.; Ernst, M.; Meier, B. H. (2019) Quantifying NMR Coherent Proton Linewidth in Proteins Under Fast MAS Conditions: A Second Moment Approach, PhysChemChemPhys (21) 18850-18865 doi: 10.1039/c9cp03414e
- Lacabanne, D.; Orelle, C.; Lecoq, L.; Kunert, B. ; Chuilon, C. ; Wiegand, T.; Ravaud, S.; Jault, J.-M. ; Meier, B. H.; Böckmann, A. (2019) Flexible-to-rigid transition is central for substrate transport in the ABC transporter BmrA from Bacillus subtilis, Commun. Biol. (2) 1-9 doi.org/10.1038/s42003-019-0390-x |
- Malär, A. A.; Dong, S.; Kehr, G.; Erker, G.; Meier, B. H.; Wiegand T. (2019) Characterization of H2-splitting products of Frustrated Lewis Pairs: Benefit of fast magic-angle spinning. ChemPhysChem, (20) 672-679 doi.org/10.1002/cphc.201900006
- Wiegand T. ; Cadalbert, R.; Lacabanne, D.; Timmins, J. ; Terradot, L. ; Böckmann, A.; Meier, B. H. (2019) The conformational changes coupling ATP hydrolysis and translocation in a bacterial DnaB helicase. Nat. Commun. (10) 31 doi:10.1038/s41467-018-07968-3
- Boudet, J.; Devillier, J.-C. ; Wiegand T.; Salmon, L.; Meier, B. H.; Lipps, G.; Allain, F. H.-T. (2019) A small helical bundle prepares primer synthesis by binding two ATP nucleotides that enhance sequence-specific recognition of the DNA template. Cell, (176) 154-166. doi.org/10.1016/j.cell.2018.11.031
Magnetische Resonanz Komplexer Materialien und Katalysatoren
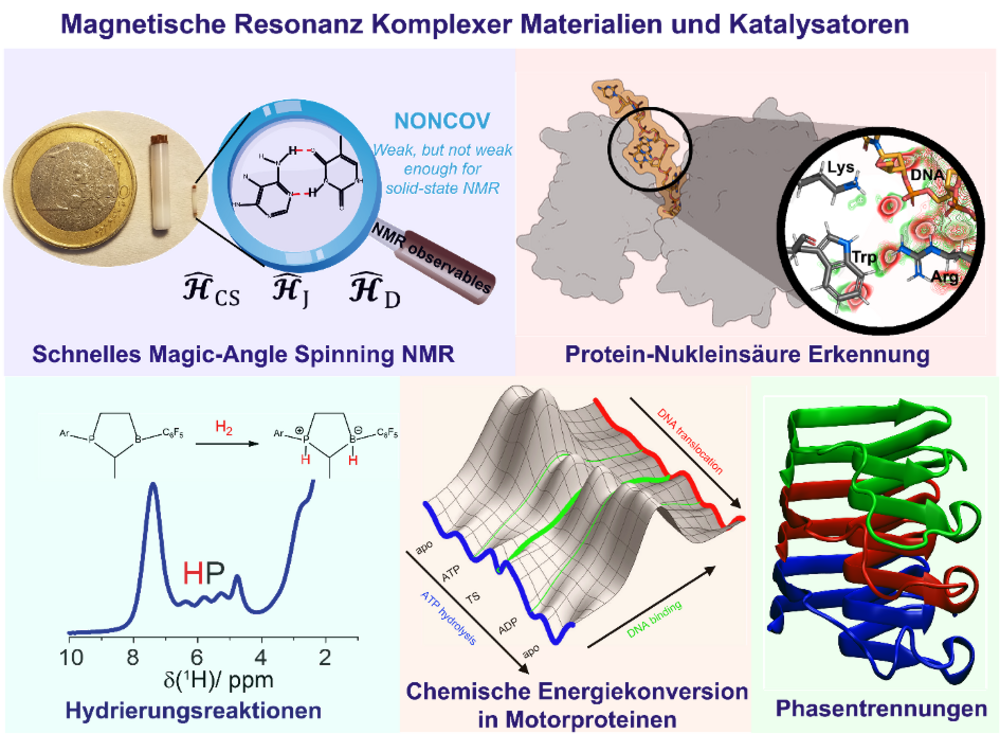
Wir bedienen uns der Magnetresonanzspektroskopie um katalytische Prozesse in der Biologie und der Chemie zu studieren und um die Rolle schwacher, nicht-kovalenter Wechselwirkungen in solchen Prozessen zu beleuchten. Insbesondere verwenden und entwickeln wir Ansätze basierend auf der Festkörper-Kernresonanzspektroskopie (NMR), die es uns sogar ermöglichen, nicht-kristalline Materialien, wie Hydrogele, amorphe Polymere, Partikel auf festen Oberflächen, Proteinfibrillen oder große Protein-Nukleinsäure-Komplexe zu untersuchen. Ein Fokus unserer Forschung liegt auf der Detektion von Protonen, die häufig zentral in einem molekularen Erkennungsprozess sind, welcher chemische Reaktionen oder Assemblierungsprozesse initiiert. Bis vor kurzem waren Protonen-detektierte Festkörper-NMR-Spektren allerdings wenig informativ, was in der geringen Auflösung begründet lag. Heutzutage verfügbare schnelle „Magic-Angle Spinning“ (MAS) Techniken mit MAS-Frequenzen größer als 100 kHz reduzieren die Linienbreiten deutlich und ermöglichen die Identifizierung und Auflösung von Protonen involviert in verschiedensten nicht-kovalenten Wechselwirkungen (wie Wasserstoffbrücken, π-π- oder hydrophobe Wechselwirkungen, etc.). Wir interpretieren unsere experimentellen Ergebnisse in Kombination mit quantenchemischen Rechnungen, um zu verstehen, wie NMR-Observablen durch nicht-kovalente Wechselwirkungen beeinflusst werden.
Unsere Vision ist es, vereinheitlichende Konzepte in der Katalyse zu entwickeln, um Unterschiede zwischen der Biologie und der Chemie zu überwinden. Unsere Strategien zur mechanistischen Untersuchung von Hydrierungsreaktionen beinhalten schnelle MAS-Experimente, sowie Hyperpolarisationsexperimente unter Verwendung von para-Wasserstoff (Para-hydrogen Induced Polarization, PHIP). Spannende Modellsysteme sind beispielsweise Frustrierte Lewis-Paare, die die Fähigkeiten besitzen, kleine Moleküle (z.B. Di-Wasserstoff) zu aktivieren oder zu binden. Im biomolekularen Kontext untersuchen wir die zelluläre Organisation durch Phasentrennungsprozesse in Proteinen, welche in Zusammenhang mit neurodegenerativen Erkrankungen stehen (z.B. RNA-bindende Proteine). Die Flüssig-flüssig-Phasentrennung wird aktuell intensiv diskutiert. Sie ermöglicht es Zellen, räumlich und zeitlich biologische Reaktionen in Unterkammern, wie membranlosen Organellen, zu regulieren. Wir entwickeln Festkörper-NMR und Elektronenspinresonanzspektroskopie (ESR) Werkzeugkästen, um insbesondere Flüssig-fest-Phasentrennungen zu untersuchen und die schwachen nicht-kovalenten Wechselwirkungen, welche als Triebkraft von Phasentrennungen angesehen werden können, zu identifizieren. Ein weiterer zentraler Fokus unserer Arbeiten liegt auf der mechanistischen Aufklärung von chemischen Energiekonversionsprozessen in Proteinen, wie ATP-angetriebenen Motorproteinen, welche in der DNA-Replikation involviert sind. Hier untersuchen wir das Binden von Nukleinsäuren an Proteine, was es uns ermöglicht, Modelle für die ATP-Hydrolyse und deren Kopplung mit der Proteinfunktionalität zu entwickeln. Diese neu etablierten Experimente werden es uns ebenfalls erlauben, die Rolle von RNA in Phasentrennungsereignissen zu untersuchen.
Wir freuen uns über Interesse von enthusiastischen Semester-, Bachelor-, Masterstudent*innen, sowie Doktorand*innen an unserer Forschung und sind sehr neugierig, Sie/euch kennenzulernen.