Dr. Alexander Schnegg - EPR Forschungsgruppe

- Dr. Alexander Schnegg
- Forschungsgruppenleiter
- EPR Research Group
- +49 (0)208 306 - 3526
- alexander.schnegg(at)cec.mpg.de
- Raum: 211
Vita
| Dipl.-Phys. | Freie Universität Berlin (1998) |
| Dr. rer. nat. | Institut für Experimentalphysik, Freie Universität Berlin (1999-2003) |
| Postdoc | Max-Planck-Institut für Bioanorganische Chemie; heute: MPI CEC (2004-2005) |
| Postdoc | Helmholtz-Zentrum Berlin für Materialien und Energie (HZB) (2006-2013) |
| Wiss. Mitarbeiter | Verantwortlicher Wissenschaftler im EPR-Labor am HZB (2013-2018) |
| Adjunct professor | Monash University, Melbourne, Australia (seit 2016) |
| Forschungsgruppenleiter | MPI CEC (seit 2018) |
Publications
Selected MPI CEC publications
- Mato, M., Bruzzese, P. C., Takahashi, F., Leutzsch, M., Reijerse, E. J., Schnegg, A., Cornella, J. (2023). Oxidative Addition of Aryl Electrophiles into a Red-Light-Active Bismuthinidene. Journal of the American Chemical Society, 145(34), 18742-18747. doi:10.1021/jacs.3c06651.
- Tran, V. A., Teucher, M., Galazzo, L., Sharma, B., Pongratz, T., Kast, S. M. M., Marx, D., Bordignon, E., Schnegg, A., Neese, F. (2023). Dissecting the Molecular Origin of g-Tensor Heterogeneity and Strain in Nitroxide Radicals in Water: Electron Paramagnetic Resonance Experiment versus Theory. The Journal of Physical Chemistry A, 127(31), 6447-6466. doi:10.1021/acs.jpca.3c02879.
- Tretiakov, S., Lutz, M., Titus, C. J., de Groot, F., Nehrkorn, J., Lohmiller, T., Holldack, K., Schnegg, A., Tarrago, M. F. X., Zhang, P., Ye, S., Aleshin, D., Pavlov, A., Novikov, V., Moret, M.-E. (2023). Homoleptic Fe(III) and Fe(IV) Complexes of a Dianionic C-3-Symmetric Scorpionate. Inorganic Chemistry, (62), 101613-10625. doi:10.1021/acs.inorgchem.3c00871.
- Rams, M., Lohmiller, T., Böhme, M., Jochim, A., Foltyn, M., Schnegg, A., Plass, W., Näther, C. (2023). Weakening the Interchain Interactions in One Dimensional Cobalt(II) Coordination Polymers by Preventing Intermolecular Hydrogen Bonding. INORGANIC CHEMISTRY, 62(26), 10420-10430. doi:10.1021/acs.inorgchem.3c01324.
- Lau, K., Niemann, F., Abdiaziz, K., Heidelmann, M., Yang, Y., Tong, Y., Fechtelkord, M., Schmidt, T. C., Schnegg, A., Campen, R. K., Peng, B., Muhler, M., Reichenberger, S., Barciowski, S. (2023). Differentiating between Acidic and Basic Surface Hydroxyls on Metal Oxides by Fluoride Substitution: A Case Study on Blue TiO2 from Laser Defect Engineering. Angewandte Chemie, International Edition in English, (62): e20221396, pp. 1-12. doi:10.1002/anie.202213968.
- Yang, X., Reijerse, E. J., Nöthling, N., SantaLucia, D., Leutzsch, M., Schnegg, A., Cornellà, J. (2023). Synthesis, Isolation, and Characterization of Two Cationic Organobismuth(II) Pincer Complexes Relevant in Radical Redox Chemistry. Journal of the American Chemical Society, (145), 5618_5623. doi:10.1021/jacs.2c12564.
- Yang, X., Reijerse, E.J., Nöthling, N., SantaLucia, D.J., Leutzsch, M., Schnegg, A., Cornella, J., (2023). Synthesis, Isolation, and Characterization of Two Cationic Organobismuth(II) Pincer Complexes Relevant in Radical Redox Chemistry. (2023) Journal of the American Chemical Society. https://doi.org/10.1021/jacs.2c12564.
- Lau, K., Niemann, F., Abdiaziz, K., Heidelmann, M., Yang, Y., Tong, Y., Fechtelkord, M., Schmidt, T. C., Schnegg, A., Campen, R. K., Peng, B., Muhler, M., Reichenberger, S., Barcikowski, S. (2023). Differentiating between Acidic and Basic Surface Hydroxyls on Metal Oxides by Fluoride Substitution: A Case Study on Blue TiO2 from Laser Defect Engineering. Angewandte Chemie International Edition, e202213968. https://doi.org/10.1002/anie.202213968.
- Larsen, E. M. H., Bonde, N. A., Weihe, H., Ollivier, J., Vosch, T., Lohmiller, T., Holldack, K., Schnegg, A., Perfetti, M., Bendix, J. (2023). Experimental assignment of long-range magnetic communication through Pd & Pt metallophilic contacts. Chemical Science, 14 (2), 266-276. doi:10.1039/d2sc05201f.
- Pohle, M.H., Böhme, M., Lohmiller, T., Ziegenbalg, S., Blechschmidt, L.; Görls, H., Schnegg, A., Plass, W. (2023). Magnetic Anisotropy and Relaxation of Pseudotetrahedral [N2O2] Bis-Chelate Cobalt(II) Single-Ion Magnets Controlled by Dihedral Twist Through Solvomorphism. Chemistry a European Journal,(29)1-7 e202202966. https://doi.org/10.1002/chem.202202966
- Sharma, M. K., Chabbra, S., Wölper, C., Weinert, H. M., Reijerse, E. J., Schnegg, A., Schulz, S. (2022). Modulating the frontier orbitals of L(X)Ga-substituted diphosphenes [L(X)GaP](2) (X = Cl, Br) and their facile oxidation to radical cations. Chemical Science, 13(43), 12643-12650. doi:10.1039/d2sc04207j.
- Yang, X., Reijerse, E. J., Bhattacharyya, K., Leutzsch, M., Kochius, M., Nöthling, N., Busch, J., Schnegg, A., Auer, A. A., Cornella, J. (2022). Radical Activation of N-H and O-H Bonds at Bismuth(II). Journal of the American Chemical Society, (144), 16535-16544. doi:10.1021/jacs.2c05882.
- Lohmiller, T., Spyra, C.-J., Dechert, S., Demeshko, S., Bill, E., Schnegg, A., Meyer, F. (2022). Antisymmetric Spin Exchange in a mu-1,2-Peroxodicopper(II) Complex with an Orthogonal Cu-O-O-Cu Arrangement and S = 1 Spin Ground State Characterized by THz-EPR. JACS Au, 2(5), 1134-1143. doi:10.1021/jacsau.2c00139.
- Teucher, M., Sidabras, J. W., Schnegg, A. (2022). Milliwatt three- and four-pulse double electron electron resonance for protein structure determination. Physical Chemistry Chemical Physics, (24), 12528-12540. doi:10.1039/d1cp05508a.
- Chatterjee, S., Harden, I., Bistoni, G., Castillo, R. G., Chabbra, S., van Gastel, M., Schnegg, A., Bill, E., Birrell, J. A., Morandi, B., Neese, F., DeBeer, S. (2022). A Combined Spectroscopic and Computational Study on the Mechanism of Iron-Catalyzed Aminofunctionalization of Olefins Using Hydroxylamine Derived N-O Reagent as the "Amino" Source and "Oxidant". Journal of the American Chemical Society, 144(6), 2637-2656. doi:10.1021/jacs.1c11083.
- Bonke, S.A., Risse, T., Schnegg A., Brückner A., (2021) In situ electron paramagnetic resonance spectroscopy for catalysis; Nature Review Methods Primers 2021 1 (1), 33. https://doi.org/10.1038/s43586-021-00031-4
- Liu, C., Geer, A. M., Webber, C., Musgrave, C., Gu, S., Johnson, G., Dickie, D. A., Chabbra, S., Schnegg, A., Zhou, H., Sun, C.-J., Hwang, S., Goddard III, W. A., Zhang, S., Gunnoe, T. B. (2021). Immobilization of "Capping Arene" Cobalt(II) Complexes on Ordered Mesoporous Carbon for Electrocatalytic Water Oxidation. ACS Catalysis, (11), 15068-1508 DOI: 10.1021/acscatal.1c04617
- Shin, D., Bhandari, S., Tesch, M. F., Bonke, S. A., Jaouen, F., Chabbra, S., Pratsch, C., Schnegg, A., Mechler, A. K. (2022). Reduced formation of peroxide and radical species stabilises iron-based hybrid catalysts in polymer electrolyte membrane fuel cells. Journal of Energy Chemistry, 65, 433-438. doi:10.1016/j.jechem.2021.05.047 .
- Büker, J., Alkan, B., Chabbra, S., Kochetov, N., Falk, T., Schnegg, A., Schulz,C., Wiggers, H., Muhler, M., Peng, B. (2021). Liquid-Phase Cyclohexene Oxidation with O-2 over Spray-Flame-Synthesized La1-xSrxCoO3 Perovskite Nanoparticles. SI, 27(68), 16912-16923. doi:10.1002/chem.202103381.
- Nehrkorn, J. P., Valuev, I. A., Kiskin, M. A., Bogomyakov, A. S., Suturina, E. A., Sheveleva, A. M., Ovcharenko, V., Holldack, K.,Herrmann, C., Fedin, M. V., Schnegg, A., Veber, S.L. (2021) Easy-plane to easy-axis anisotropy switching in a Co(ii) single-ion magnet triggered by the diamagnetic lattice. Journal of Materials Chemistry C, 9(30), 9446, 1-7. doi:10.1039/d1tc01105g.
- Ott, J. C., Suturina, E. A., Kuprov, I., Nehrkorn, J., Schnegg, A., Enders, M., Lutz, H.G. (2021). Observability of paramagnetic NMR signals at over 10 000 ppm chemical shifts. Angewandte Chemie, International Edition, (60), 22856-22864. doi:10.1002/anie.202107944.
- Zhao, G., Bonke, S. A., Schmidt, S., Wang, Z., Hu, B., Falk, T., Hu, Y., Rath, T ., Xia, W ., Peng, B., Schnegg, A., Weng, Y., Muhler, M.(2021). Highly Efficient and Selective Aerobic Oxidation of Cinnamyl Alcohol under Visible Light over Pt-Loaded NaNbO3 Enriched with Oxygen Vacancies by Ni Doping. ACS Sustainable Chemistry & Engineering, 9(15), 5422-5429. doi:10.1021/acssuschemeng.1c00460.
- Shin, D., Bhandari, S., Tesch, M. F., Bonke, S. A., Jaouen, F., Chabbra, S., Pratsch, C., Schnegg, A., Mechler, A.K. (2022). Reduced formation of peroxide and radical species stabilises iron-based hybrid catalysts in polymer electrolyte membrane fuel cells. Journal of Energy Chemistry, 65, 433-438. doi.org/10.1016/j.jechem.2021.05.047 .
- Bone, A. N., Widener, C. N., Moseley, D. H., Liu, Z., Lu, Z., Cheng, Y., Daemen, L. L, Ozerov, M.,Telser, J., Thirunavukkuarasu, K., Smirnov, D., Greer, S. M., Hill, Stephen., Krzystek, J., Holldack, K., Aliabadi, A., Schnegg, A., Dunbar, K. R., Xue, Zi-Ling (2021). Applying Unconventional Spectroscopies to the Single-Molecule Magnets, Co(PPh3)(2)X-2 (X=Cl, Br, I): Unveiling Magnetic Transitions and Spin-Phonon Coupling. Chemistry – A European Journal, 27, 11110. doi:10.1002/chem.202100705.
- Tarrago, M., Römelt, C., Nehrkorn, J., Schnegg, A., Neese, F., Bill, E., Ye, S. (2021). Experimental and Theoretical Evidence for an Unusual Almost Triply Degenerate Electronic Ground State of Ferrous Tetraphenylporphyrin. Inorganic chemistry, 60(7), 4966-4985. doi:10.1021/acs.inorgchem.1c00031.
- Nehrkorn, J. P., Greer, S. M., Malbrecht, B. J., Anderton, K. J., Azat Aliabadi, K., Schnegg, A., Holldack, K., Herrmann, C., Betley, T., Stoll, S., Hill, S. (2021). Spectroscopic Investigation of a Metal–Metal-Bonded Fe6 Single-Molecule Magnet with an Isolated S = 19/2 Giant-Spin Ground State. Inorganic Chemistry, 60(7), 4610-4622. doi:10.1021/acs.inorgchem.0c03595.
- Pavlov, A.A., Nehrkorn, J., Zubkevich, S.V., Fedin, M.V., Holldack, K., Schnegg, A., Novikov, V.V. (2020). A Synergy and Struggle of EPR, Magnetometry and NMR: A Case Study of Magnetic Interaction Parameters in a Six-Coordinate Cobalt(II) Complex Inorganic Chemistry 59(15), 10746-10755. https://doi.org/10.1021/acs.inorgchem.0c01191.
- Viciano-Chumillas, M., Blondin, G., Clémanceym N., Krzystek, J., Ozerov, M., Armentano, D., Schnegg, A., Lohmiller, T., Telser, J., Lloret, F., Cano, J. (2020). Single‐Ion Magnetic Behaviour in an Iron(III) Porphyrin Complex: A Dichotomy Between High‐Spin and 5/2−3/2 Spin Admixture Chemistry – A European Journal 26(62), 14242-14251. https://doi.org/10.1002/chem.202003052.
- Jochim, A., Lohmiller, T., Rams, M., Böhme, M., Ceglarska, M., Schnegg, A., Plass, W., Näther, C. (2020). Influence of the Coligand onto the Magnetic Anisotropy and the Magnetic Behavior of One-Dimensional Coordination Polymers Inorganic Chemistry 59(13), 8971-8982. https://doi.org/10.1021/acs.inorgchem.0c00815.
- Lin, Y.-H., Kutin, Y., van Gastel, M., Bill, E., Schnegg, A., Ye, S., Lee, W.-Z. (2020). A Manganese(IV)-Hydroperoxo Intermediate Generated by Protonation of the Corresponding Manganese(III)-Superoxo Complex Journal of the American Chemical Society 11(24), 15068-15082. https://doi.org/10.1021/jacs.0c02756.
- Böhme, M., Jochim, A., Rams, M., Lohmiller, T., Suckert, S., Schnegg, A., Plass, W., Näther, C. (2020). Variation of the Chain Geometry in Isomeric 1D Co(NCS)2 Coordination Polymers and Their Influence on the Magnetic Properties Inorganic Chemistry 59(8), 5325-5338. https://doi.org/10.1021/acs.inorgchem.9b03357.
- Ma, Y., Pang, Y., Chabbra, S., Reijerse, E.J., Schnegg, A., Niski, J., Leutzsch, M., Cornella, J. (2020). Radical C‒N Borylation of Aromatic Amines Enabled by a Pyrylium Reagent Chemistry – A European Journal 26(17), 3734-3743. https://doi.org/10.1002/chem.202000412.
- Krzystek, J., Schnegg, A., Aliabadi, A., Holldack, K., Stoian, S.A., Ozarowski, A., Hicks, S.D., Abu Omar, M.M., Thomas, K.E., Ghosh, A., Caulfield, K.P., Tonzetich, Z.J., Telser, J. (2020). Advanced Paramagnetic Resonance Studies on Manganese and Iron Corroles with a Formal d4 Electron Count Inorganic Chemistry 59(2), 1075-1090. https://doi.org/10.1021/acs.inorgchem.9b02635.
- Li, J., Chen, J., Sang, R., Ham, W.-S., Plutschack, M.B., Berger, F., Chabbra, S., Schnegg, A., Genicot, C., Ritter, T. (2020). Photoredox catalysis with aryl sulfonium salts enables site-selective late-stage fluorination Nature Chemistry 12, 56-62. https://doi.org/10.1038/s41557-019-0353-3.
- Rams, M., Jochim, A., Böhme, M., Lohmiller, T., Ceglarska, M., Rams, M.M., Schnegg, A., Plass, W., Näther, C. (2020). Single‐Chain Magnet Based on Cobalt(II) Thiocyanate as XXZ Spin Chain Chemistry – A European Journal 26(13), 2837-2851. https://doi.org/10.1002/chem.201903924.
- Kutin, Y., Cox, N., Lubitz, W., Schnegg, A., Rüdiger, O. (2019). In Situ EPR Characterization of a Cobalt Oxide Water Oxidation Catalyst at Neutral pH Catalysts 9(11), 926. https://doi.org/10.3390/catal9110926.
- Nehrkorn, J., Bonke, S.A., Aliabadi, A., Schwalbe, M., Schnegg, A. (2019). Examination of the Magneto-Structural Effects of Hangman Groups on Ferric Porphyrins by EPR Inorganic Chemistry 58(20), 14228-14237. https://doi.org/10.1021/acs.inorgchem.9b02348.
- Sidabras, J., Duan, J., Winkler, M., Happe, T., Hussein, R., Zouni, A., Suter, D., Schnegg, A., Lubitz, W., Reijerse, E.J. (2019) Extending electron paramagnetic resonance to nanoliter volume protein single crystals using a self-resonant microhelix Science Advances 5(10), eaay1394. https://doi.org/10.1126/sciadv.aay1394.
- Cheng, J., Liu, J., Leng, X., Lohmiller, T., Schnegg, A., Bill, E., Ye, S., Deng, L. (2019). A Two-Coordinate Iron(II) Imido Complex with NHC Ligation: Synthesis, Characterization, and Its Diversified Reactivity of Nitrene Transfer and C–H Bond Activation Inorganic Chemistry 58, 7634-6744. https://doi.org/10.1021/acs.inorgchem.9b01147.
- Zhao, G., Busser, G.W., Froese, C., Hu, B., Bohnke, S.A., Schnegg, A., Ai, Y., Wei, D., Wang, X., Peng, B., Muhler, M. (2019). Anaerobic Alcohol Conversion to Carbonyl Compounds Over Nanoscaled Rh-doped SrTiO3 under Visible Light The Journal of Physical Chemistry Letters 10, 2075–2080. https://doi.org/10.1021/acs.jpclett.9b00621.
- Nehrkorn, J., Veber, S.L., Zhukas, L.A., Novikov, V.N., Nelyubina, Y.V., Voloshin, Y.Z, Holldach, K., Stoll, S., Schnegg, A. (2018). Determination of Large Zero-Field Splitting in High-Spin Co(I) Clathrochelates Inorganic Chemistry 57(24), 15330-15340. https://doi.org/10.1021/acs.inorgchem.8b02670.
Gruppenmitglieder
EPR Forschungsgruppe am MPI CEC
Die EPR-Forschungsgruppe am MPI CEC nutzt die electron paramagnetic resonance (EPR, im Deutschen häufig Elektronenspinresonanz (ESR) genannt) als spektroskopische Methode zur Identifizierung und Charakterisierung paramagnetischer Zustände in Prozessen, die für die Energiekonversion und –speicherung relevant sind. Ein spezielles Augenmerk gilt katalytisch aktiven Übergangsmetallionen und Radikalen. Die Gruppe entwickelt und benutzt EPR-Spektrometer der neuesten Generation im Frequenzbereich von einigen GHz bis zu mehreren THz. Unsere Spektrometer erlauben eine Vielzahl spezifischer Experimente im Puls- und Dauerstrichbetrieb, darunter Doppelresonanz- und Multi-Frequenz-Experimente für Kristalle, Lösungen, Festkörper und in-situ-Experimente.
Momentan sind wir in den folgenden Forschungsfeldern aktiv:
In-situ EPR
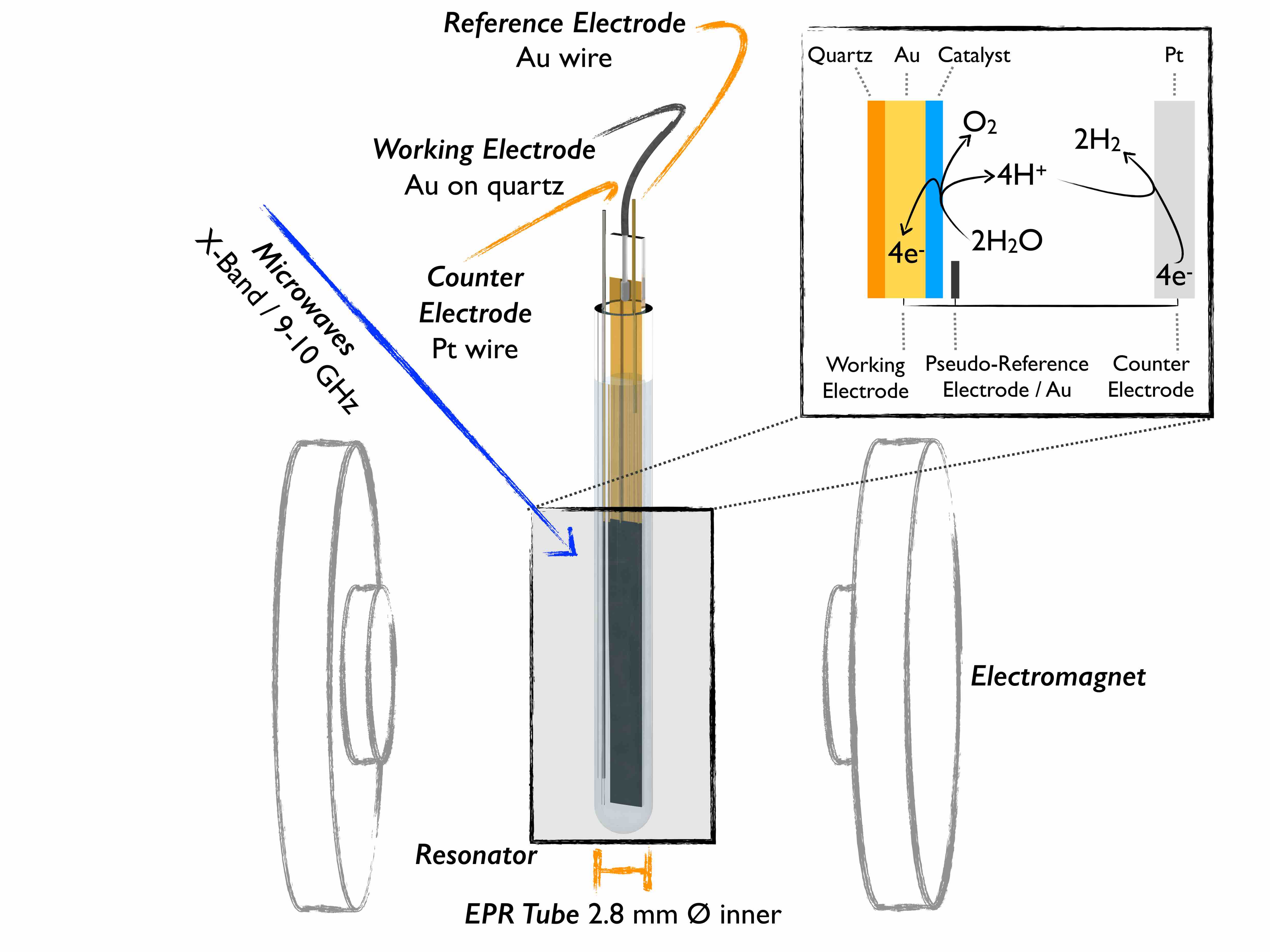
Die wissensbasierte Veränderung und Verbesserung von Katalysatoren erfordern ein tiefgreifendes Verständnis ihrer Funktionsmechanismen. Jedoch werden die reaktivsten katalytischen Zustände häufig erst während der Reaktion gebildet und sind somit nur unter Reaktionsbedingungen zu analysieren. Diesem Umstand begegnen wir mit der Entwicklung und Anwendung von in-situ/operando-EPR-Methoden. Diese Studien erfordern die Konstruktion elektrochemischer Zellen innerhalb eines EPR-Probenröhrchens (siehe Abb. 2) und den Einsatz von Durchflusssystemen im EPR-Spektrometer. Dabei stehen unter anderem Reaktionen für die elektrokatalytische Wasseroxidation mit dünnen Übergangsmetallionenfilmen oder homogenen Katalysatoren im Mittelpunkt. Spektro-elektrochemische EPR wird im Rahmen des DFG-Sonderforschungsbereichs (SFB) 247 zur Untersuchung paramagnetischer Zustände in Co-Oxid-Katalysatoren für Alkoholoxidationsreaktionen und im SFB 1487 zur Charakterisierung Eisen in Hochspinzustände in Einzelatomkatalysatoren für die Sauerstoffreduktionsreaktionen eingesetzt.
Bonke, S. A.; Risse, T.; Schnegg, A.; Brückner, A. (2021) In situ electron paramagnetic resonance spectroscopy for catalysis. Nature Review Methods Primers, https://doi.org/10.1038/s43586-021-00031-4
Kontakt: Dr. Kaltum Abdiaziz
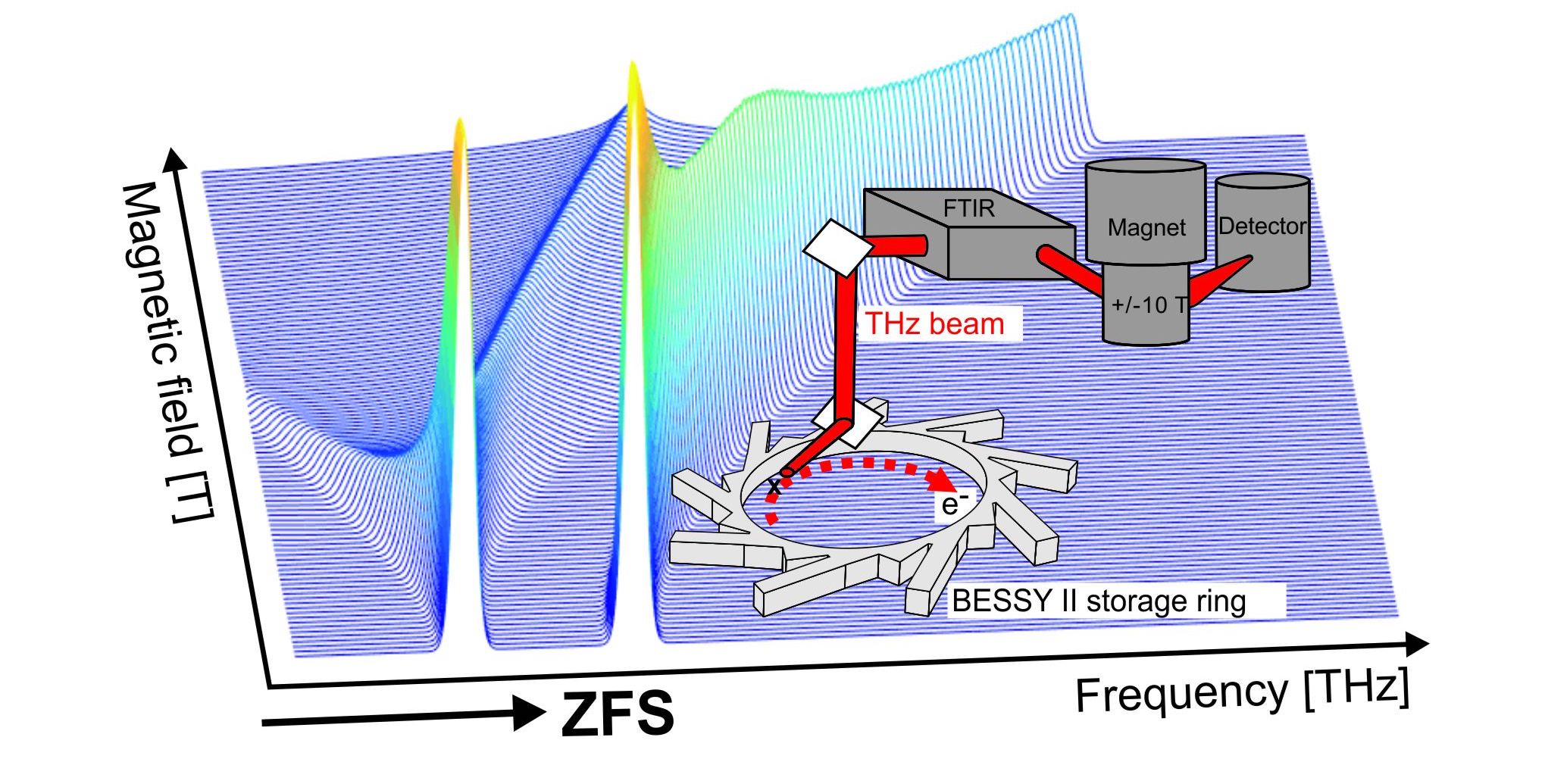
Übergangsmetallionen in Hochspinzuständen
Das Ziel von EPR-Messungen an Hochspinzuständen (S > 1/2) von Übergangsmetallionen ist die Bestimmung ihrer Spinkopplungsparameter. Letztere sind empfindliche Sonden der Koordinationsumgebung und der elektronischen Struktur, die sowohl die magnetischen als auch die chemischen Eigenschaften des Ions bestimmen. Im Falle katalytisch aktiver Übergangsmetalle können die Kopplungen einzigartige Informationen über den Struktur-Funktions-Zusammenhang liefern, wobei vor allem die sogenannten Nullfeldaufspaltungen der Elektronenspins entscheidende Informationen enthalten. Jedoch sind diese Parameter mit herkömmlichen Spektrometern häufig nicht zugänglich. Um diese Lücke zu schließen entwickelt die EPR-Gruppe neuartige Hochfrequenz/Hochfeld-Spektrometer mit Anwendungsenergien bis in den THz-Bereich und setzt sie für Studien an einer Vielzahl katalytisch relevanter Hochspinsysteme (u.a. FeII,III,IV, CoIII, NiI, MnIII,IV) ein.
Lohmiller, T.; Spyra, C.-J.; Dechert, S.; Demeshko, S.; Bill, E.; Schnegg, A.; Meyer, F. (2022) Antisymmetric Spin Exchange in a μ-1,2-Peroxodicopper(II) Complex with an Orthogonal Cu–O–O–Cu Arrangement and S = 1 Spin Ground State Characterized by THz-EPR. JACS Au, https://doi.org/10.1021/jacsau.2c00139
Kontakt: Dr. Alexander Schnegg
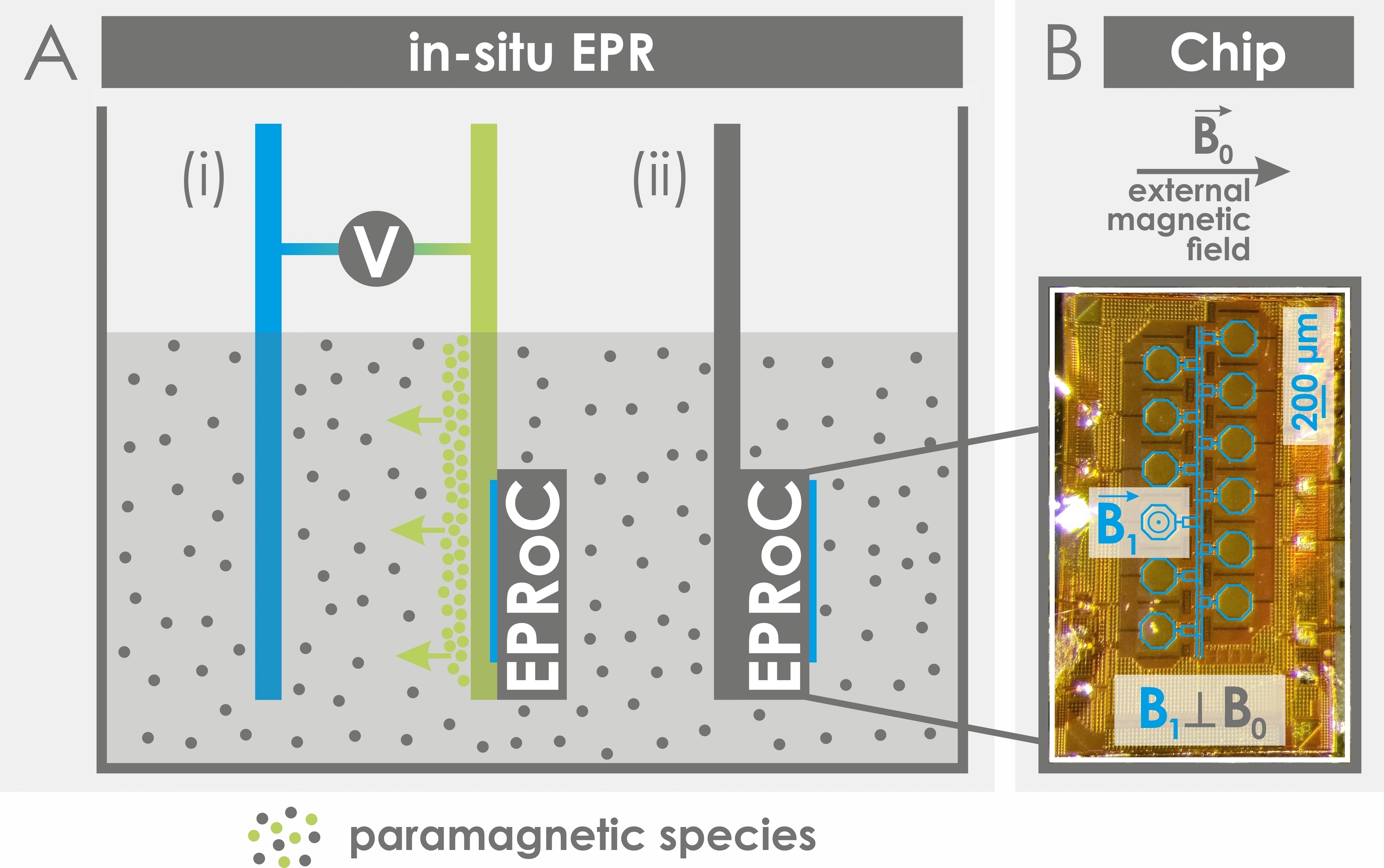
EPR-on-a-Chip (EPRoC)
EPRoC sind mm-große Sensoren, die eine Mikrowellenquelle und einen -detektor auf einem Halbleiterchip enthalten und einen grundlegenden Paradigmenwechsel in der EPR-Spektroskopie einleiten, indem sie in-situ-Messungen von paramagnetischen Proben in miniaturisierten Aufbauten auf kosteneffiziente Weise ermöglichen. Wir entwickeln EPR-Detektionsschemata, bei denen EPRoC-Sensoren, die in der Anders Gruppe (Universität Stuttgart) entwickelt werden, in verschiedenen Umgebungen eingesetzt werden, um paramagnetische Zustände mit Relevanz für die Katalyse- und Batterieforschung zu untersuchen. Dabei sind wir an ihrer Integration in Elektroden von elektrochemischen Experimenten interessiert. Die Forschung mit EPRoC-Sensoren wird vom Bundesministerium für Bildung und Forschung gefördert (Förderkennzeichen: 03SF0565A).
Kontakt: Dr. Takuma Sato
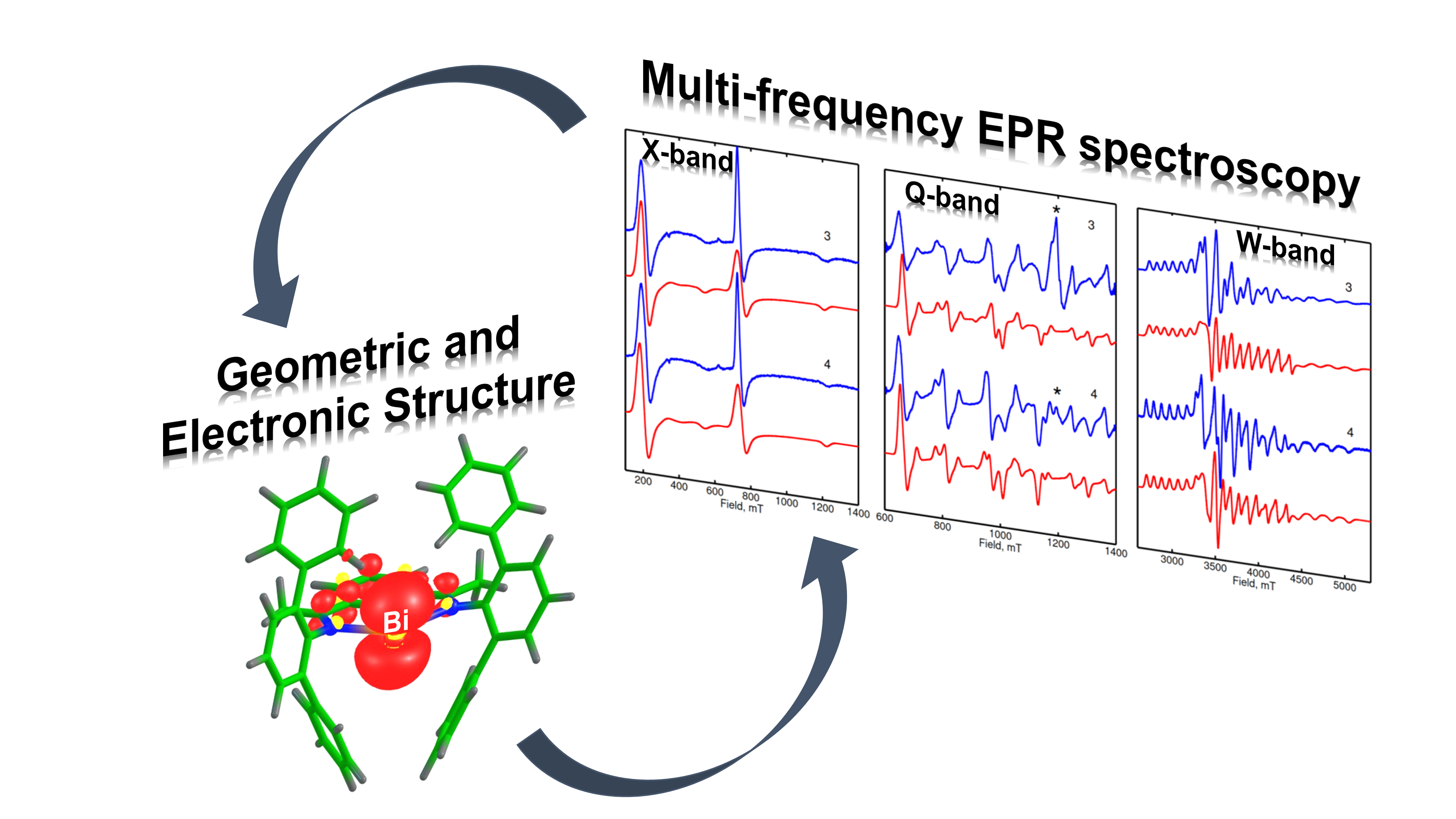
Charakterisierung aktiver Zentren mit Multifrequenz-EPR- und Hyperfeinspektroskopie
Die Identifizierung und Charakterisierung katalytisch aktiver Zentren ist zentral für das Verständnis katalytischer Prozesse. Aktive Zentren sind häufig paramagnetisch. Sie können daher hervorragend mit Hilfe der EPR-Spektroskopie untersucht werden, die wichtige Details ihrer geometrischen und elektronischen Struktur liefert. In unserer Gruppe werden hochauflösende Multifrequenz- (S-, X-, Q- und W-Band) und Multiresonanz-EPR-Techniken eingesetzt, um funktionsrelevante Informationen in den verschiedenen Zweigen der Katalyse zu erhalten, die von der homogenen Katalyse über die heterogene Katalyse bis zu heterogenisierten Einzelatomkatalysatoren reichen. Mit Hilfe der Hyperfeinspektroskopie (HYSCORE, ENDOR und EDNMR) nutzen wir Kernspins um die erste und zweite Koordinationssphäre aktiver Zentren zu charakterisieren. Dadurch können spezifische Merkmale der chemischen Bindungen beleuchtet werden, die für das Verständnis der katalytischen Eigenschaften aktiver Zentren entscheidend sind. Die Verbindung der katalytischen und chemischen Eigenschaften einerseits mit den durch die EPR ermittelten Spineigenschaften andererseits erfolgt mit Hilfe modernster quantenchemischer Methoden. Auf diese Weise werden Struktur-Eigenschafts-Korrelationen gewonnen.
Yang, X.; Reijerse, E. J.; Bhattacharyya, K.; Leutzsch, M.; Kochius, M.; Nöthling, N.; Busch, J.; Schnegg, A.; Auer, A. A.; Cornella, J. (2022) Radical Activation of N–H and O–H Bonds at Bismuth(II). Journal of the American Chemical Society, https://doi.org/10.1021/jacs.2c05882
Lin, Y.-H.; Kutin, Y.; van Gastel, M.; Bill, E.; Schnegg, A.; Ye, S.; Lee, W.-Z. (2020) A Manganese(IV)-Hydroperoxo Intermediate Generated by Protonation of the Corresponding Manganese(III)-Superoxo Complex. Journal of the American Chemical Society, https://doi.org/10.1021/jacs.0c02756
Kontakt: Dr. Edward J. Reijerse und Dr. Paolo Cleto Bruzzese